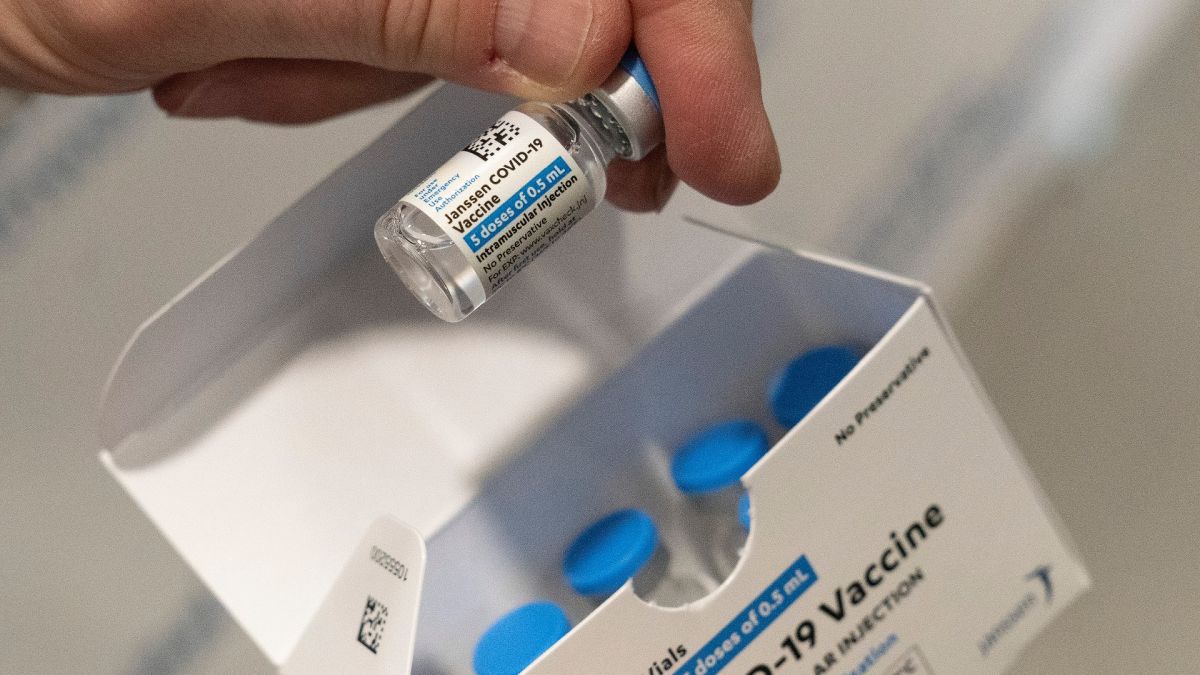
Szczepionka firmy Janssen (której macierzystą firmą jest Johnson & Johnson) uzyskała warunkowe pozwolenie na dopuszczenie do obrotu w Islandii. Europejska Agencja Leków zarekomendowała warunkowe dopuszczenie jej do obrotu, co potwierdziła Komisja Europejska. Jest to czwarta szczepionka przeciwko COVID-19 dopuszczona do obrotu na Islandii i w pozostałych krajach Europy. Różni się ona od innych tym, że wymagana jest tylko jedna dawka, a nie dwie, jak w przypadku pozostałych szczepionek.
Ta szczepionka jest przeznaczona dla osób w wieku co najmniej 18 lat. Została poddana badaniom klinicznym w USA, Afryce Południowej i Ameryce Południowej, w których wzięło udział ponad 44 000 uczestników. Wyniki wskazują, że zapewnia ona ochronę przed wirusem na poziomie 67%. Najczęściej występujące efekty uboczne były łagodne lub umiarkowane, obejmowały bolesność w miejscu wstrzyknięcia, ból głowy, zmęczenie, ból mięśni i nudności, i mijały w ciągu kilku dni. Bezpieczeństwo i skuteczność szczepionki są stale monitorowane zarówno przez firmę farmaceutyczną, jak i Europejską Agencję Leków.
Profesor immunologii z Uniwersytetu Islandzkiego, Ingileif Jónsdóttir, powiedziała dla RÚV, że badania wykazały, iż szczepionka Janssen chroni również przed południowoafrykańskim, jak i brazylijskim wariantem wirusa. Jej skuteczność wynosiła ponad 63% we wszystkich grupach wiekowych i płciach, u osób z różnych środowisk, jak również u osób z chorobami współistniejącymi. Stwierdziła, że skuteczność szczepionki jest dość wysoka po jednym zastrzyku, ale trwają dalsze badania, aby ustalić, czy drugi zastrzyk zwiększy skuteczność, tak jak w przypadku szczepionki firmy AstraZeneca.
Islandzka służba zdrowia zamówiła 235 000 dawek szczepionki Janssen, jednak nie opublikowano jeszcze harmonogramu jej dystrybucji.
W przypadku każdej szczepionki obowiązuje 7 etapów dopuszczenie jej do użycia:
- Unia Europejska podpisuje umowę z daną firmą farmaceutyczną
- Zostaje ukończona faza III prób klinicznych
- Islandia podpisuje umowę dotyczącą danej szczepionki
- Komisja Europejska dopuszcza szczepionkę do obrotu
- Islandzka Agencja Leków dopuszcza szczepionkę do obrotu w Islandii
- Szczepionka jest sprowadzana do Islandii
- Rozpoczynają się szczepienia daną szczepionką
Pfizer – BioNTech (szczepionka mRNA)**
Islandia podpisała umowę z firmą Pfizer w dniu 9 grudnia 2020 r. oraz dodatkowe umowy w dniach 30 grudnia 2020 r. i 8 marca 2021 r. Komisja Europejska i Islandzka Agencja Leków (IMA) wydały warunkowe pozwolenie na dopuszczenie szczepionki do obrotu. Islandia otrzyma około 410 000 dawek, co wystarczy dla około 205 000 osób. Szczepionka została dostarczona do Islandii 28 grudnia, a szczepienia rozpoczęły się 29 grudnia 2020 r.
Moderna (szczepionka mRNA)**
Islandia podpisała umowę z firmą Moderna w dniu 30 grudnia. Komisja Europejska i Islandzka Agencja Leków wydały warunkowe pozwolenie na dopuszczenie do obrotu. Islandia otrzyma ok. 128 tys. dawek, co wystarczy dla ok. 64 tys. osób.
Astra Zeneca – Oxford (szczepionka wektorowa)*
Islandia podpisała umowę z firmą Astra Zeneca w dniu 15 października. Komisja Europejska i Islandzka Agencja Leków wydały warunkowe pozwolenie na dopuszczenie do obrotu. Islandia otrzyma około 230 000 dawek, co wystarczy do zaszczepienia około 115 000 osób.
Janssen – Johnson & Johnson (szczepionka wektorowa)*
Islandia podpisała umowę z firmą Janssen w dniu 22 grudnia. Komisja Europejska i Islandzka Agencja Leków wydały warunkowe pozwolenie na dopuszczenie do obrotu. Islandia otrzyma szczepionkę dla około 235 000 osób. Dostawa szczepionki ma się rozpocząć w drugim kwartale 2021 roku.
CureVac (szczepionka mRNA)**
Islandia podpisała umowę z CureVac 21 lutego. Ocena Europejskiej Agencji Leków jest warunkiem wstępnym do uzyskania pozwolenia na dopuszczenie do obrotu. Islandia otrzyma szczepionkę dla około 90 000 osób. Dostawa szczepionki ma się rozpocząć w drugim kwartale 2021 roku.
Sanofi (szczepionka proteinowa)***
Negocjacje w sprawie tej szczepionki jeszcze się nie rozpoczęły. Informacje na temat liczby dawek dla Islandii nie są dostępne. Nadal nie ma pewności co do czasu rejestracji i dostawy, ale można założyć, że nastąpi to najwcześniej w czwartym kwartale 2021 roku.
*Szczepionka tego typu jest oparta na wektorach, czyli fragmentach aktywnych wirusów, które zostały poddane modyfikacji, aby wywołać odpowiedź immunologiczną przeciw wirusowi SARS-CoV-2.
**W tym rodzaju szczepionki kwas rybonukleinowy (RNA) jest wykorzystywany jako matryca do produkcji białek wirusowych, które mają za zadanie wywołać produkcję przeciwciał, przekazywanych następnie do układu immunologicznego osoby zaszczepionej.
***W tego rodzaju szczepionce do wywołania reakcji immunologicznej jest wykorzystywane białko z powierzchni wirusa.